Tak, niestety, Twoje zwierzę również jest narażone na ryzyko zarażenia się COVID-19. Podobnie jak my jesteśmy podatni na zakażenie wirusem SARS-CoV-2, niektóre gatunki zwierząt również. Ponieważ zwierzęta mają podobne cechy strukturalne białek powierzchniowych komórek obecnych u ludzi.
Specyficzne obecne białko działa jak system zamka i klucza, kluczem jest białko wirusa odpowiedzialne za infekcję COVID-19, a zamkiem jest białko błonowe znajdujące się na powierzchni komórki.
Jeśli klucz - białko wirusa - pasuje do zamka - białka receptora gospodarza - wówczas wirus może dostać się do środka, rozpoczynając cykl namnażania, powodując infekcję gospodarza.
Badanie opublikowane na stronie PLOS Computational Biologywykorzystali model matematyczny do przewidywania, które gatunki zwierząt mają niezbędne cechy białka gospodarza, które mogłyby umożliwić wiązanie białka kolca wirusa.
Naukowcy zgłosili kilka przypadków na całym świecie, w których zwierzęta domowe, hodowlane i z ogrodów zoologicznych uzyskały pozytywny wynik testu na zakażenie COVID-19.
Koty, norki, lwy i tygrysy to niektóre gatunki, które zostały zarażone.
Początkowo badania wykazały, że koty, cywety i fretki były podatne na SARS-CoV-2, podczas gdy świnie, kurczaki i kaczki nie.
W drugim momencie pojawiły się inne wyniki, klasyfikujące świnki morskie, myszy i szczury jako niepodatne, podczas gdy wielbłądy, bydło, konie, owce i króliki zostały sklasyfikowane jako podatne na zakażenie SARS-CoV-2.
Należy pamiętać, że wirus SARS-CoV-2 został po raz pierwszy przeniesiony na ludzi przez żywiciela pośredniego.
Dwa główne podejrzane zwierzęta to nietoperze i pangoliny. Jeśli po raz pierwszy słyszysz o pangolinach, są to nocne ssaki pokryte keratynowymi łuskami, które żyją w wydrążonych drzewach i norach.
Oto ilustracja przedstawiająca pangolina:
Aby rozpocząć infekcję, pierwszym krokiem, jaki musi wykonać wirus, jest związanie jego białka kolca wirusowego z białkiem receptora z błony komórkowej gospodarza.
Białko receptora gospodarza jest zewnątrzkomórkową domeną proteazy enzymu konwertującego angiotensynę 2, zwykle znanego jako ACE2.
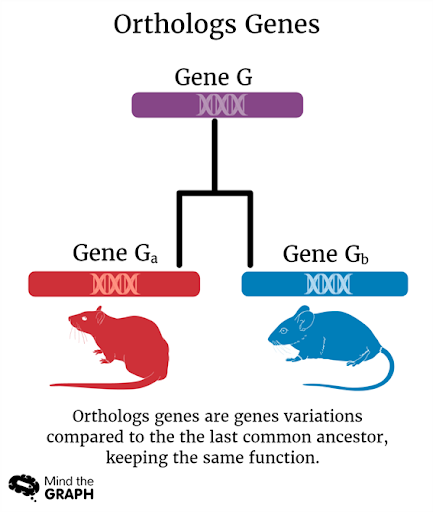
ACE2 jest jednoprzebiegowym białkiem transmembranowym obecnym na powierzchni kilku tkanek. ACE2 nie ma tylko jednej struktury, może mieć wiele struktur międzygatunkowych, zachowując tę samą funkcję.
W rzeczywistości ACE2 jest klasyfikowany jako gen ortologiczny, czyli gen obecny u różnych gatunków, który pochodzi od wspólnego genu przodka.
Te różnice strukturalne są najwyraźniej powodem, dla którego wirus SARS-CoV-2 może wiązać się z ACE2 niektórych gatunków, a nie innych.
Gdy wirusowe białko kolca zostanie połączone z ACE2, wirus dostaje się do wnętrza komórki i zaczyna wykorzystywać maszynerię komórkową gospodarza do namnażania się, co prowadzi do infekcji.
W rezultacie lepsze zrozumienie receptora ACE2 z pewnością doprowadziłoby do bardziej precyzyjnego wyjaśnienia, dlaczego niektóre gatunki zwierząt są podatne na infekcje, podczas gdy inne nie.
Ponadto pomogłoby to również naukowcom w opracowywaniu leków, stosując strategie przeciwwirusowe, takie jak wytwarzanie fałszywych blokad do wiązania się wirusa zamiast rzeczywistej blokady gospodarza.
Jak również w celu lepszego śledzenia pośrednich zwierząt-gospodarzy pod kątem przyszłych infekcji wirusowych.
Tak więc, scharakteryzowanie trójwymiarowej struktury ACE2 i jego interakcji na poziomie atomowym przy użyciu modelowania obliczeniowego, było celem projektu. Rodrigues i współpracownicy praca.
Tego typu badania charakteryzujące są kosztowne eksperymentalnie i nie mają zastosowania na dużą skalę, co utrudnia uzyskanie rozstrzygających danych, tymczasem modelowanie obliczeniowe jest szybkie i niedrogie, co jest bardzo korzystne dla wypełnienia pewnych luk w wiedzy o strukturze.
W badaniu wzięto do analizy 28 gatunków zwierząt, generując model 3D ACE2 połączonego z wirusowym białkiem kolca.
Wyniki wykazały, że istnieją kluczowe miejsca w sekwencji aminokwasowej ACE2, w których z powodu mutacji białko wirusowe nie może wiązać się z komórką gospodarza.
W szczególności, w sekwencji ACE2 brakuje jednego aminokwasu odpowiedzialnego za międzycząsteczkowy mostek solny obserwowany między ACE2 a miejscem wiązania białka wirusowego, jak donosi Rodrigues i jego zespół.
Wynik ten jest poparty innymi opublikowanymi badaniami, które wykazały eksperymentalnie, że brak tego mutanta jest brakiem ujemnie naładowanego aminokwasu, umożliwiającego wiązanie białka wirusowego.
Badanie wskazuje również, że infekcja SARS-CoV-2 jest bardziej złożona niż wcześniej sądzono, z więcej niż jednym sposobem zarażenia gospodarza.
Dlatego ważne jest, aby wyjaśnić, że zmniejszenie dostępności ACE2 może zmniejszyć szanse na infekcję; nie zapobiega to jednak wystąpieniu infekcji.
I że modele obliczeniowe nie mogą być wykorzystywane samodzielnie do przewidywania ryzyka zakażenia gatunków - aby uzyskać bardziej wiarygodne wnioski, konieczne są dodatkowe dane eksperymentalne.
Myślę więc, że musimy nadal postępować zgodnie z protokołami pandemicznymi i robić to, co już robiliśmy... Używać masek, utrzymywać dystans społeczny tak bardzo, jak to możliwe, nie chodzić do pomieszczeń zamkniętych i zatłoczonych, dla naszego bezpieczeństwa, a zwłaszcza naszych ukochanych zwierząt domowych, nas samych i naszej rodziny.
Ten puszysty kot jest taki piękny, prawda? Tę i wiele innych ilustracji zwierząt można znaleźć na platformie Mind the Graph.
Weterynaria, ornitologia, entomologiaoraz zoologia Na platformie dostępne są również ilustracje, które można wykorzystać w swojej infografice. Zacznij korzystać z Mind the Graph teraz!

Zapisz się do naszego newslettera
Ekskluzywne, wysokiej jakości treści na temat skutecznych efektów wizualnych
komunikacja w nauce.