Oxid uhličitý je běžný plyn přítomný v atmosféře. Koloběh uhlíku na Zemi za normálních okolností udržuje přirozenou rovnováhu uhlíku v atmosféře, na pevnině a v oceánech prostřednictvím "dýchání planety". Lidská činnost v podobě emisí fosilních paliv však narušuje rovnováhu uhlíkového cyklu a způsobuje změnu klimatu, neboť zvyšuje skleníkový efekt a okyselování oceánů.
Abychom pochopili důsledky okyselování oceánů, musíme si nejprve zrekapitulovat koloběh uhlíku. O tom jsem psal zde1.
Skleníkový efekt umožňuje život na Zemi tím, že zachycuje teplo v atmosféře a otepluje planetu. Jak to funguje, jsem ukázal zde1. Navzdory jejímu významu se však v důsledku zvyšujícího se množství oxidu uhličitého stala problémem.
Ne všechen přebytečný oxid uhličitý však zůstává v atmosféře. Vědci odhadují, že oceány pohltily třetinu veškerého oxidu uhličitého vyprodukovaného lidskou činností. Odstraňování oxidu uhličitého z atmosféry oceánem pomáhá oddálit rozsah klimatických změn. Tento přínos má však svou cenu.
Oxid uhličitý a chemie oceánu
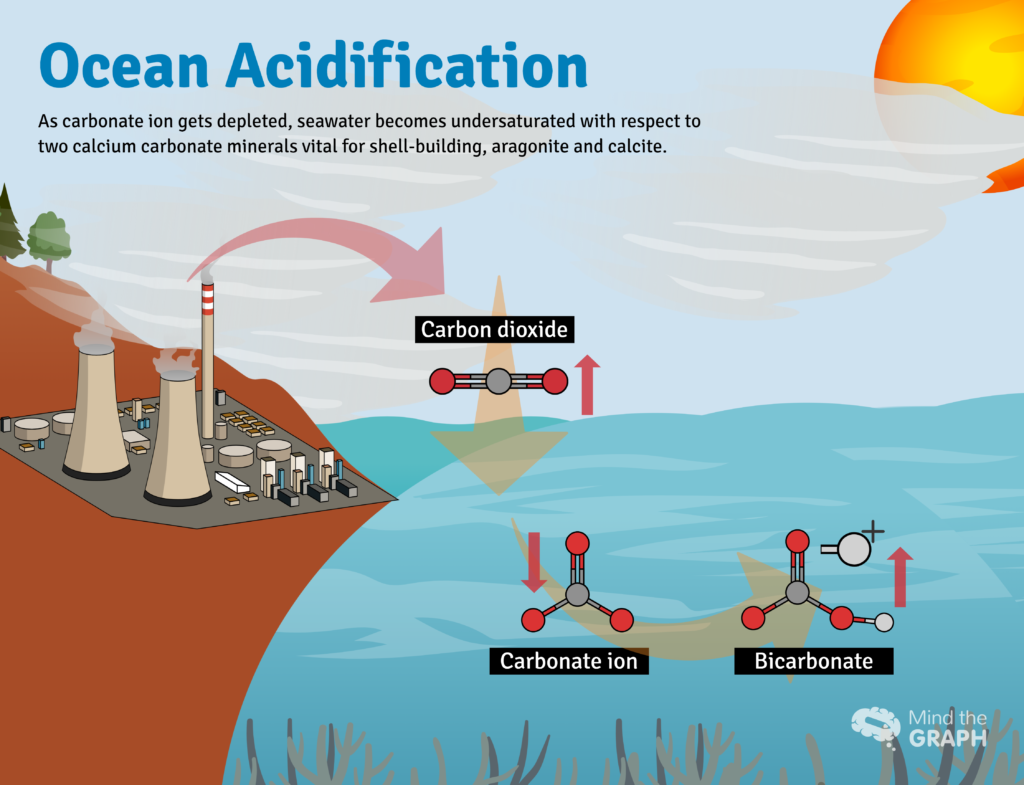
Po rozpuštění v mořské vodě reaguje CO2 s vodou (H2O) za vzniku kyseliny uhličité: H2CO3: CO2 + H2O ↔ H2CO3. Kyselina uhličitá se rychle rozpouští za vzniku iontů H+ (kyselina) a hydrogenuhličitanu HCO3- (zásada). Mořská voda je přirozeně nasycena další zásadou, uhličitanovým iontem (CO3-2), který působí jako antacidum, neutralizuje H+ a vytváří další hydrogenuhličitan. Čistá reakce vypadá následovně: CO2 + H2O + CO3-2→ 2HCO3-
Absorpce oxidu uhličitého zásadně mění chemické složení oceánů tím, že vyvolává reakce, při nichž se mořská voda stává kyselejší, což je jev nazývaný okyselování oceánů. Oceán se ve skutečnosti stal téměř o 30 % kyselejší než na počátku průmyslové éry. Jde o změnu větší a rychlejší, než jaká je patrná ve fosilních záznamech starých nejméně 800 000 let, tedy před výskytem obratlovců a rostlin ve fosilních záznamech.
Jaký dopad bude mít okyselování oceánů na mořské živočichy, jako jsou ryby, korály a měkkýši?
S rostoucí koncentrací vodíkových iontů se voda stává kyselejší. Kromě toho ubývá uhličitanových iontů.
Některé z dodatečných vodíkových iontů reagují s uhličitanovými ionty za vzniku dalších hydrogenuhličitanů. S úbytkem uhličitanů mají tyto organismy, jako jsou koráli a mlži, větší potíže se stavbou a udržováním svých schránek a koster. Zvýšená kyselost může dokonce způsobit, že se některé uhličitanové schránky a kostry rozpustí. Vodíkové ionty reagují s pevným uhličitanem vápenatým a přeměňují ho na rozpustný hydrogenuhličitan a vápenaté ionty.
Mezi směsicí drobných rostlin a živočichů, kteří tvoří plankton, žije drobný mořský plž zvaný pteropod. Navzdory své malé velikosti jsou pteropodi důležitým zdrojem potravy pro mnoho druhů, včetně ryb, tuleňů a velryb. Pteropodi však mají křehké schránky z uhličitanu vápenatého, které jsou zranitelné vůči okyselování oceánů. V sérii experimentů byly schránky pteropodů umístěny do mořské vody o pH (kyselosti), které se předpokládá pro Jižní oceán v roce 2100. Během 48 hodin se skořápky pteropodů začaly rozpouštět.
Vizualizace výzkumu
Vizuální zdroje, jako jsou infografiky a videa, jsou účinným způsobem, jak informovat o vědě. Všechny tyto infografiky jsem vytvořil pomocí online platformy Mind the graph, která vědcům umožňuje vytvářet poutavé materiály.

Přihlaste se k odběru našeho newsletteru
Exkluzivní vysoce kvalitní obsah o efektivním vizuálním
komunikace ve vědě.